আলোচ্য বিষয় গ্যাসের আচরণ দশম শ্রেণী প্রশ্ন উত্তর ও গ্যাসের আচরণ গাণিতিক সমস্যা। WBBSE নির্ধারিত সিলেবার অনুযায়ী টপিক ধরে আলোচনা। মাধ্যমিকে ভালো নম্বর পেতে আমার নোটটি পড়তেই হবে।
অধ্যায় : গ্যাসের আচরণ দশম শ্রেণী প্রশ্ন উত্তর
গ্যাসের আচরণ সংক্রান্ত বিভিন্ন টপিক অনুযায়ী আলোচনা ও তার প্রশ্ন- উত্তর গুলি সাজিয়ে দেওয়া হল।
গ্যাসের আচরণ সংক্রান্ত বিভিন্ন ভৌতরাশির একক:
গ্যাসের আচরণ সংক্রান্ত সূত্রাবলী :
আদর্শ গ্যাসের সমীকরণঃ
PV = nRT যেখানে, P= গ্যাসের চাপ, V= গ্যাসের আয়তন, n= মোলসংখ্যা, T= উষ্ণতা, R= সার্বজনীন গ্যাস ধ্রুবক।
R এর CGS এককে মান = 8.314 × 10¹⁰ আর্গ.মোল⁻¹.কেলভিন⁻¹
R এর SI এককে মান = 8.314 জুল.মোল⁻¹.কেলভিন⁻¹
R এর Lit.atm এককে মান = 0.082 Lit.atm.মোল⁻¹.কেলভিন⁻¹–এই মানটি গাণিতিক সমস্যায় ব্যবহার করবে,
তবে তখন গ্যাসের চাপ কে atm(বায়ুমন্ডলীয় চাপ) এককে ও আয়তনকে Lit.(লিটার) এককে লিখতে হবে।
এবিষয়ে মনে রাখবে,
1 atm = 76 cm পারদস্তম্ভের(Hg) চাপ = 760 mm পারদস্তম্ভের(Hg) চাপ
1 Lit = 1000 cc বা cm³ = 1000 ml
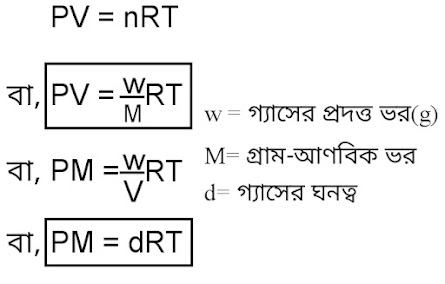
আদর্শ গ্যাস সমীকরণের ভিন্ন রূপগুলিঃ
গ্যাসের আচরণ গাণিতিক সমস্যা
গ্যাসের আচরণ গাণিতিক সমস্যা গুলি মাধ্যমিক পরীক্ষায় যেরূপ আসে তার নমুণা দেওয়া হল। টেস্ট -পেপার বা অন্যান্য প্রাক্টিস পেপার থেকে অংক গুলো প্রাক্টিস করা বিশেষ প্রয়োজন।
প্র: 4 অ্যাটমস্ফিয়ার চাপে ও 300K উয়তায় ৪g H, গ্যাসের (H1) আয়তন কত হবে? (R = 0.082 L.atm.mol⁻¹.K⁻¹)
উঃ প্রদত্ত,
চাপ, P = 4 atm
উষ্ণতা, T = 300K
ভর, W= 8 g
গ্রাম-আণবিক ভর,M= 1 × 2 = 2 g
R = 0.082 L.atm.mol⁻¹.K⁻¹
আয়তন, V = ?
আমরা জানি, PV = w/M.RT
বা, V =( 8×0.082×300) / (2×4) = 6.15 Lit
প্রঃ 300K উদ্ধৃতায় 760 mm Hg চাপে কোনো গ্যাসের আয়ত্ন 300 cm³। STP তে এই গ্যাসের আয়তন কত হবে?
উঃ প্রদত্ত, প্রাথমিক চাপ, P₁ = 760 mm Hg
প্রাথমিক আয়তন, V₁ = 300 cm³
প্রাথমিক উষ্ণতা, T₁ = 300 K
অন্তিম চাপ, P₂ = 760 mm Hg (STP)
অন্তিম উষ্ণতা,T₂ = 273 K (STP)
সুতরাং, অন্তিম আয়তন, V₂= ?
(*একই রাশির প্রাথমিক ও অন্তিম অবস্থার একক গুলি একই হতে হবে)
আমরা জানি, P₁V₁ / T₁ = P₂V₂ / T₂
বা, V₂ = P₁V₁T₂/ T₁P₂ = ( 760×300×273) / (300×760) = 273 cm³
প্রঃ 300 K উন্নতায় 570 mm Hg চাপে 2.2g CO গ্যাসের আয়তন নির্ণয় । [C= 12, O=16] (R = 0.082 L.atm.mol⁻¹.K⁻¹)
উঃ প্রদত্ত,
চাপ, P = 570 mm Hg চাপ = 560/760 atm = ¾ atm
উষ্ণতা, T = 300K
গ্যাসের ভর, W= 2.2 g
CO₂ এর গ্রাম-আণবিক ভর,M= 12 + 16×2 = 44 g
R = 0.082 L.atm.mol⁻¹.K⁻¹
আয়তন, V = ?
আমরা জানি, PV = w/M.RT
বা, V = 1.64 Lit
গ্যাসের আচরণ দশম শ্রেণী প্রশ্ন উত্তর
গ্যাসের আচরণ দশম শ্রেণী প্রশ্ন উত্তর হিসেবে কিছু সত্য ও মিথ্যা নির্বাচন করা দেওয়া হল যা মাধ্যমিক পরীক্ষায় আসে।
সত্য/মিথা লেখোঃ
1. একই উদ্ভূতা ও চাপে সমআয়তন CO₂ ও N₂ গ্যাসের মধ্যে অণুর সংখ্যা পৃথক।-মিথ্যা
2. অ্যাভোগাড্রো সূত্রে গ্যাসের অণুগুলির আয়তন গণ্য করা হয়।-মিথ্যা
3. আদর্শ গ্যাসের বাস্তবে কোনো অস্তিত্ব নেই।-সত্য
4. গ্যাসীয় পদার্থের অণুগুলির মধ্যে আন্তরাণবিক আকর্ষণ বর্তমান।-সত্য
5. গ্যাসীয় পদার্থের অণুগুলির নির্দিষ্ট আয়তন থাকে।-সত্য
6. উষ্ণতা বৃদ্ধিতে গ্যাসের আয়তন পূর্বের আয়তনের 1/273 অংশে বৃদ্ধি পায়।-সত্য
7. বাস্তবে পরমশূন্য উষ্ণতা পাওয়া সম্ভব নয় ।-সত্য
৪. উষ্ণতা বৃদ্ধি করলে গ্যাসীয় পদার্থের অণুগুলির গতিশক্তি বৃদ্ধি পায়।-সত্য
9. PV = KT-কে আদর্শ গ্যাস সমীকরণ বলে। -মিথ্যা (বয়েল ও চার্লসের সূত্রের সমন্বয় সূত্র বলে)
10. নির্দিষ্ট উষ্ণতা ও চাপে কোনো আবদ্ধ পাত্রে রক্ষিত গ্যাসের মধ্যে অণুগুলির বেগ সমান।-সত্য
গ্যাসের আচরণ দশম শ্রেণী প্রশ্ন উত্তর হিসেবে কিছু শূণ্যস্থান পূরণ ও তার উত্তর দেওয়া হল যা মাধ্যমিক পরীক্ষায় আসে।
শূন্যস্থান পূরণ:
1. স্থির তাপমাত্রায় নির্দিষ্ট ভরের কোনো গ্যাসের ক্ষেত্রে চাপ ও আয়তনের গুণফল সর্বদা ___________।
2. বয়েলের সূত্রানুসারে P-V লেখচিত্রকে________ বলে।
3. বায়ুমণ্ডলের চাপ পরিমাপ করা হয়________ সাহায্যে।
4. শুষ্ক বায়ু অপেক্ষা আর্দ্র বায়ু ______হয়।
5. 1 বার = _____N.m-2
6. গ্যাস অণুগুলির গড় গতিশক্তি ওই গ্যাসের পরম উন্নতার______।
উত্তরঃ 1. ধ্রুবক। 2. সমোয়রেখা। 3. ব্যারোমিটারের। 4. হালকা। 5.10⁵। 6. সমানুপাতিক ।
গ্যাসের আচরণ দশম শ্রেণী প্রশ্ন উত্তর হিসেবে কিছু গুরুত্বপূর্ণ প্রশ্ন ও উত্তর দেওয়া হল যা মাধ্যমিক পরীক্ষায় আসে।
প্রঃ বয়েলের সূত্রটি বিবৃত করো। বয়েলের সূত্রের গাণিতিক রূপ?বেলুনে ফুঁ দিলে বেলুনের আয়তন বাড়ে এবং চাপও বাড়ে। এখানে বয়েলের সূত্রটি কী লঙ্ঘিত হয় ?
Ans: বিবৃতি : নির্দিষ্ট উন্নতায় নির্দিষ্ট ভরের গ্যাসের আয়তন গ্যাসের চাপের সঙ্গে। ব্যস্তানুপাতে পরিবর্তিত হয়।
গাণিতিক রূপঃ
PV = K (K=সমানুপাতিক ধ্রুবক)
অথবা,P₁V₁= P₂V₂
নির্দিষ্ট উষ্মতায় বেলুনে ফুঁ দিলে অর্থাৎ বাতাস ভর্তি করলে বেলুনের আয়তন বৃদ্ধির সঙ্গে সঙ্গে ওর ভেতরের বায়ুর চাপও বৃদ্ধি পায়। অর্থাৎ এক্ষেত্রে বেলুনের মধ্যে বায়ুর ভর স্থির থাকে না, বরং বৃদ্ধি পায়। বয়েলের সূত্র কেবলমাত্র নির্দিষ্ট ভরের গ্যাসের ক্ষেত্রেই প্রযোজ্য। সুতরাং এক্ষেত্রে আপাতভাবে বয়েলের সূত্র লঙ্ঘিত হচ্ছে বলে মনে হলেও, আদৌ সূত্রটি প্রযোজাই নয়।
প্রঃ চার্লসের সূত্রটি বিবৃত করো। গাণিতিক রূপটি লেখো।
উঃ স্থির চাপে নির্দিষ্ট ভরের কোনো গ্যাসের আয়তন প্রতি 1°C বৃদ্ধি বা হ্রাস করলে ওই গ্যাসের 0°C উয়তার আয়তনের 273 অংশ বৃদ্ধি বা হ্রাস পাবে।
Ans : (i) প্রতিটি গ্যাস অসংখ্য ক্ষুদ্রাতিক্ষুদ্র অণু দ্বারা গঠিত।
(ii) গ্যাস অণুগুলি নিরেট, গোলাকার, স্থিতিস্থাপক।
(iii) গ্যাস অণুগুলি বিন্দুভর, এই কারণে গ্যাসের আয়তনের ক্ষেত্রে অনুগুলির আয়তনকে অগ্রাহ্য করা হয়। না।
(iv) গ্যাসীয় অণুগুলির মধ্যে কেন্দ্রের আকর্ষণ বা বিকর্ষণ কাজ করে।
(v) অণুগুলি সরলরৈখিক পথে বিশৃঙ্খলভাবে সর্বদা সঞ্চরণশীল।
(vi) দ্রুত বেগে চলতে চলতে পাত্রের দেওয়ালে অনবরত ধাক্কা খায়। আবার নিজেদের মধ্যেও সংঘর্ষ ঘটে, এক্ষেত্রে প্রতিটি সংঘর্ষ স্থিতিস্থাপক।
(vii) গ্যাস অণুগুলির পরম তাপমাত্রার সমানুপাতিক।
(viii) একই গ্যাসের অণুগুলি একই রকম হয়।
কেনভিন উষ্ণতা(পরম উষ্ণতা স্কেল) = (সেলসিয়াস স্কেলে উষ্ণতা + 273)
প্রঃ 30°C ও 300K এর মধ্যে কোন তাপমাত্রাটি বেশি?
উঃ 30°C = (30 + 273) K = 303 K,৷ সুতরাং 30°C বেশি।
প্রঃ পরমশূণ্য উষ্ণতা কাকে বলে ?
উঃ যে উষ্ণতায় সকল গ্যাসের আয়তন শূন্য হয়ে যায়, তাকে পরম শূন্য উষ্ণতা বলে। সেলসিয়াস স্কলে এই পরম উষ্ণতার মান -273°C।
প্রঃ স্থির চাপে কত ডিগ্রি সেলসিয়াস উন্নতায় চার্লস সূত্র অনুসারে কোনো আদর্শ গ্যাসের আয়তন শূন্য হবে?
উঃ -273°C উষ্ণতা।
প্রঃ পরম শূন্য উষ্ণতাকে পরম বলার কারন কি?
উঃ এর থেকে কম উষ্ণতা পাওয়া সম্ভব নয় বলে।
প্রঃ কেলভিন স্কেল কী?
উঃ উষ্ণতার যে স্কেলে -273°C-কে নিম্ন-স্থিরাঙ্ক এবং প্রতি ডিগ্রির মানকে সেলসিয়াস স্কেলের এক ডিগ্রির সমান ধরা হয়, তাকে পরম উষ্ণতার স্কেল বা কেলভিন স্কেল বলে।
প্রঃ STP বা NTP-তে কোনো গ্যাসের মোলার আয়তন কত ?
উঃ 22.4 লিটার
প্রঃ মোলার আয়তন কাকে বলে ?
উঃ STP বা NTP তে এক মোল কোনো গ্যাস যে আয়তন দখল করে তাকে মোলার আয়তন বলে। STP বা NTP-তে কোনো গ্যাসের মোলার আয়তন 22.4 লিটার হয়।
প্রঃ গ্যাসের অণুর গতির ওপর উষ্ণতা হ্রাস ও বৃদ্ধির প্রভাব কী ?
উঃ উষ্ণতার সাথে গ্যাসের অণুর গতির সমানুপাতিক সম্পর্ক, অর্থাৎ উষ্ণতা বৃদ্ধিতে গ্যাসের অণুর গতি বাড়ে এবং উষ্ণতা হ্রাসে গ্যাসের অণুর গতি কমে।
প্রঃ গ্যাসের অণুগুলির গতির ওপর গ্যাসের চাপ কীভাবে নির্ভর করে?
উঃ গ্যাসের অণুগুলির গতি বৃদ্ধি পেলে গ্যাসের চাপও বৃদ্ধি পায় এবং অণুগুলির গতি হ্রাস পেলে গ্যাসের চাপও হ্রাস পায়।
প্রঃ গ্যাসের চাপের উপর উষ্ণতার প্রভাব কী ?
উঃ উষ্ণতার সাথে গ্যাসের চাপের সমানুপাতিক সম্পর্ক। উষ্ণতা বৃদ্ধিতে গ্যাসের চাপ বৃদ্ধি এবং উষ্ণতা হ্রাসে গ্যাসের চাপ হ্রাস পায়।
প্রঃ অ্যাভোগাড্রো সূত্র বা প্রকল্পটি বিবৃত করো? সূত্রটির দুটি অনুসীদ্ধান লেখো।
উঃ চাপ ও উষ্ণতা স্থির রেখে সম আয়তন সকল গ্যাসে সম সংখ্যক গ্যাস অণু পাওয়া যাবে।
অনুসীদ্ধান্তঃ
১) নিষ্ক্রিয় গ্যাস ব্যতীত সব মৌলিক গ্যাসের(হাইড্রোজেন, অক্সিজেন ইত্যাদি) অণু দ্বি-পরমাণুক।
২)গ্যাসীয় পদার্থের আণবিক ভর গ্যাসটির বাষ্পঘনত্বের দ্বিগুন।
প্রঃ বাস্তব গ্যাসগুলির আদর্শ আচরণ থেকে বিচ্যুতির কারনগুলি লেখো ?
অথবা, বাস্তব গ্যাসগুলি কেন আদর্শ গ্যাস সমীকরণ মেনে চলে না?
উঃ চাপত্রুটিঃ গ্যাসের গতীয় তত্ত্ব অনুযায়ী, অণুগুলির মধ্যে কোনো আকর্ষণ বা বিকর্ষণ বল কাজ করে না। কিন্তু বাস্তবে পাত্রের দেওয়াল সংলগ্ন অণুগুলি ভেতরের দিকে টান অনুভব করে। এ কারণে আদর্শ গ্যাসের তুলনায় বাস্তব গ্যাসের চাপ কম হয়।
আয়তন ত্রুটিঃ গ্যাসের গতীয় তত্ত্ব অনুযায়ী, গ্যাস অণুগুলি বিন্দুভর হওয়ায়, গ্যাস অণুগুলির আয়তন অগ্রাহ্য করা হয়, ফলতঃ গ্যাস অণুগুলির জন্য সমগ্র পাত্র বিচক্ষণযোগ্য। কিন্তু বাস্তব গ্যাসের অণুগুলি ক্ষুদ্র হলেও, আয়তন নগণ্য নয়। বাস্তব গ্যাস অণুগুলির অবাধ বিচরণের জন্য কার্যকরী আয়তন পাত্রের আয়তনের তুলনায় কিছু কম হয়।
প্রঃ কোন শর্তে বাস্তব গ্যাস আদর্শ গ্যাস সমীকরণ মেনে চলবে?
উঃ উচ্চ উষ্ণতা ও নিম্ন চাপে প্রায় সকল বাস্তব গ্যাস, আদর্শ গ্যাস সমীকরণ মেনে চলে।

_1%E0%A6%B8%E0%A7%8D%E0%A6%AB%E0%A6%97.jpg)